Depuis longtemps l'industrie utilise des catalyseurs pour accéléler des réactions chimiques.
Depuis longtemps l'industrie utilise des catalyseurs pour accéléler des réactions chimiques.
- On veut comparer l'efficacité d'une enzyme à celle d'un catalyseur minéral.
Notions évoquées dans ce dossier
- un catalyseur
- la catalyse
- un catalyseur minéral, biologique
- une enzyme
- un réactif, un produit
- un substrat
Source : http://www.educauto.org/ressources-mediatheque/catalyseur-dechappement
Document 1 - Notion de catalyse
La catalyse est l’action par laquelle une substance (appelée catalyseur) accélère une réaction chimique par sa seule présence, en se retrouvant intacte à l’issue de celle-ci.
Par exemple, en notant R1 et R2 deux réactifs et P le produit issu de leur combinaison, on obtient comme équation bilan :
R1 + R2 + catalyseur -> P + catalyseur
Dans un organisme, ce sont des protéines qui réalisent la catalyse : les enzymes, appelées pour cette raison des « catalyseurs biologiques ». Il existe également des catalyseurs minéraux utilisés dans l'industrie (nickel, acide chlorhydrique…).
Par exemple, l’hydrolyse de l’amidon des féculents est catalysée par l’amylase, une enzyme sécrétée par les glandes salivaires et le pancréas.
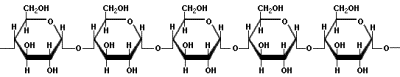
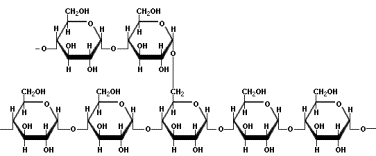
Document 2 - Amidon, amylose et amylopectine
Composition chimique de l'amidon
|
L'amidon est un mélange de deux glucides complexes, l’amylose (20%) et l’amylopectine (80%). L'amylopectine est ramifiée alors que l'amylose ne l'est pas. Les deux molécules ont pour formule brute [C6H10O5]n, n étant compris entre 200 et 20000 pour l'amylose et pouvant atteindre 2.106 pour l'amylopectine.
|
Remarque : le glycogène est formé d’amylopectine très ramifiée, mais dont les branches ne comptent pas plus de 13 résidus (jusqu’à 30 dans l’amylopectine de l’amidon).
Source : http://www.scientificpsychic.com/fitness/carbohydrates.html
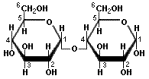
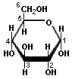
Dégradation de l'amidon par hydrolyse
|
En présence d'eau, l'amidon peut être dégradé au cours d'une réaction chimique qui sépare les résidus en rompant les liaisons au niveau de l'atome d'oxygène. Il se forme alors du maltose et un peu de glucose. |
- logiciel de simulation (Philippe Cosentino)
Pistes d'exploitation
- Lancer le logiciel, ajouter des molécules d'enzyme (amylase) et de substrat (amylose).
- Lancer le logiciel et observer la formation de molécules de produit.
- Modifier les paramètres pour optimiser la réaction chimique (obtenir la plus grande production de produit).
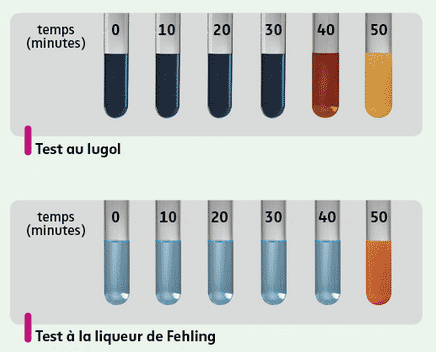
Document 3 - Comparaison de la catalyse par un catalyseur minéral et par une enzyme
Catalyse par l'acide chlorhydrique
 |
|
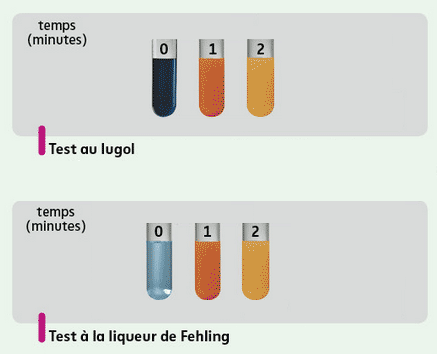
Catalyse par une enzyme
 |
|
Source (illustration): Nathan page 124
- correction du QCM (pdf)
- Ne pas confondre "réactif" (au départ d'une réaction chimique) et "réactif coloré" (ne participant pas à la réaction mais permettant de mettre en évidence certaines substances).