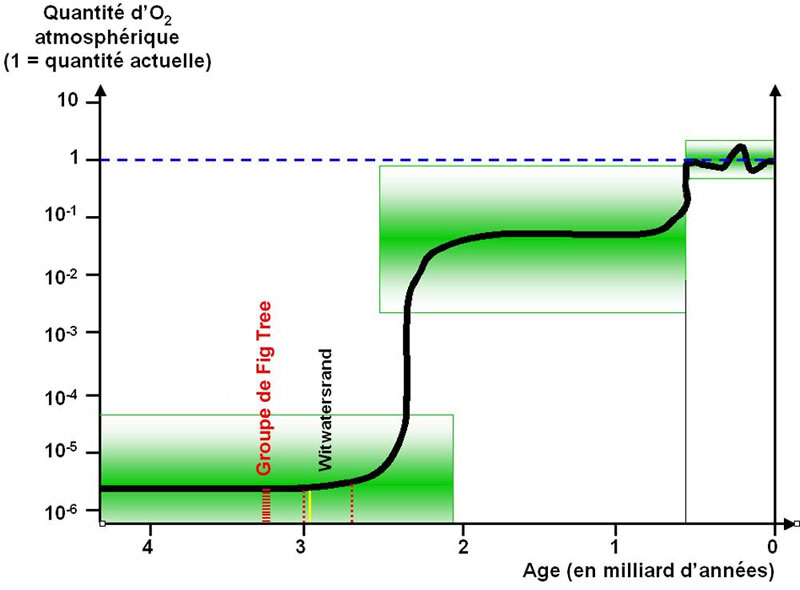
 L'évolution de la teneur de l'atmosphère en dioxygène est l'objet de nombreuses incertitudes. Le modèle présenté ici synthétise les données et les incertitudes (déterminées en 2008).
L'évolution de la teneur de l'atmosphère en dioxygène est l'objet de nombreuses incertitudes. Le modèle présenté ici synthétise les données et les incertitudes (déterminées en 2008).La plupart des gens pense que la vie ne peut se développer sur une planète que si son atmosphère contient du dioxygène. Vraiment ?
 L'évolution de la teneur de l'atmosphère en dioxygène est l'objet de nombreuses incertitudes. Le modèle présenté ici synthétise les données et les incertitudes (déterminées en 2008).
L'évolution de la teneur de l'atmosphère en dioxygène est l'objet de nombreuses incertitudes. Le modèle présenté ici synthétise les données et les incertitudes (déterminées en 2008).
Le trait noir et la zone vert foncé indiquent la valeur « probable » de cette teneur. Les rectangles verts indiquent le domaine d'incertitude où pourrait se trouver la valeur réelle.
La « brusque » augmentation du dioxygène atmosphérique vers -2,5 Ga pourrait avoir été moins brutale que dessinée ici et s'être poursuivie jusque vers –2 Ga.
Source : d'après planet-terre
Les fers rubanés ("banded iron formation" ou BIF en Anglais) constituent l'essentiel des gisements de minerai de fer du monde.
|
Ce sont des roches sédimentaires d'origine marine formées de lits d'hématite (Fe2O3) alternant avec des lits de silice (SiO2) plus ou moins colorés par l'hématite. L'hématite, normalement grise, devient rouge lorsqu'elle est hydratée (sous forme d'oxydes ferriques Fe3+). Les BIF proviennent probablement de l'activité photosynthétique de cyanobactéries, libérant des molécules de dioxygène dans l'eau. Source : planet-terre |
Le dioxygène est un oxydant fort qui peut réagir avec de nombreuses espèces chimiques dites réductrices au cours d'une réaction d’oxydoréduction. Le fer peut ainsi réagir avec le dioxygène et former des oxydes de fer (de formule générale et pouvant être rouges). Trois oxydes de fer (Fe2O3, FeO et Fe3O4) peuvent se former avec des proportions différentes de dioxygène.
On veut caractériser les divers oxydes de fer.
Source : Chemistry Channel
Source : COURS-SvT-LORITZ-CD
Ce document représente l'importance des gisements de fers rubanés depuis 4 Ga :
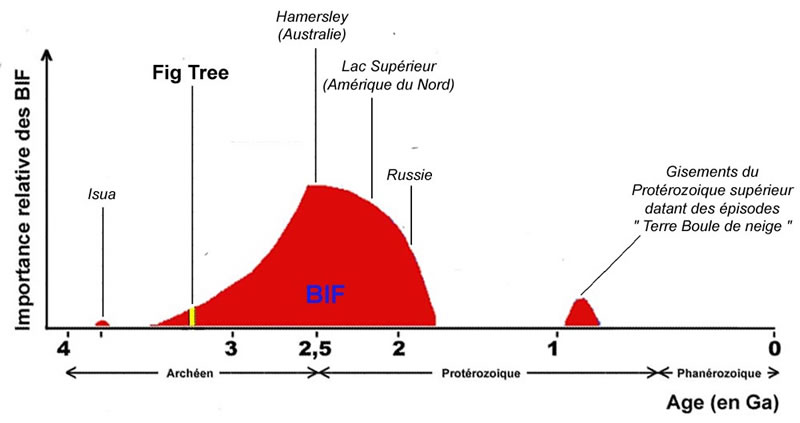
Source : ibid
Visionnez la vidéo suivante jusqu'à la 46'00.
Source : "Planète miracle", épisode "La mer primitive" (NHK - Antenne 2, 1987)
 |
On trouve sur la plage de Shark Bay en Australie, des roches particulières, les stromatolithes. Ces roches ont une forme de boule ou de champignon. Leur surface est gluante. Source : http://cas.bellarmine.edu/tietjen/Evolution/stromatolites2.htm |
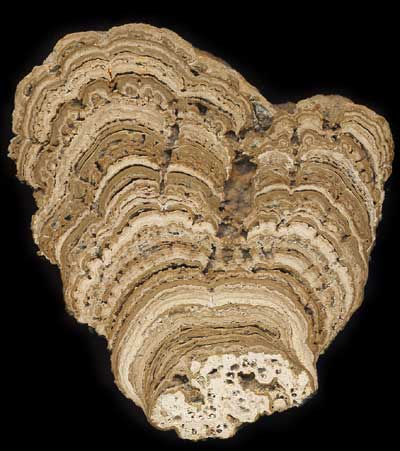 |
En coupe, elles apparaissent formées de très fines couches concentriques (stromato = couche et lithe = pierre). L'échantillon mesure quelques dizaines de cm de hauteur. Les trous visibles à la base sont des loges de larves d'insectes qui vivent dans une eau très peu profonde (les phryganes). Source : www.mnhn.fr/mnhn/mineralogie/histoire/index/collections/sedimentaires.htm Les stromatolithes se forment grâce à l'activité de cyanobactéries. On peut les observer au microscope en prélevant un échantillon dans une stromatolithe (actuelle ou fossile). |
| Cyanobactéries fossiles (ME) | Cyanobactéries actuelles (MO) |
|---|---|
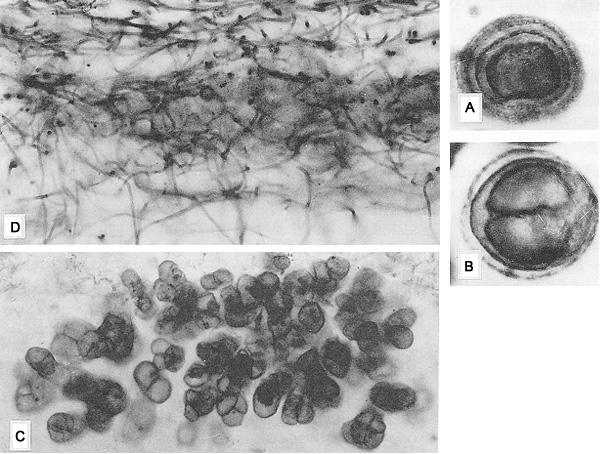 |
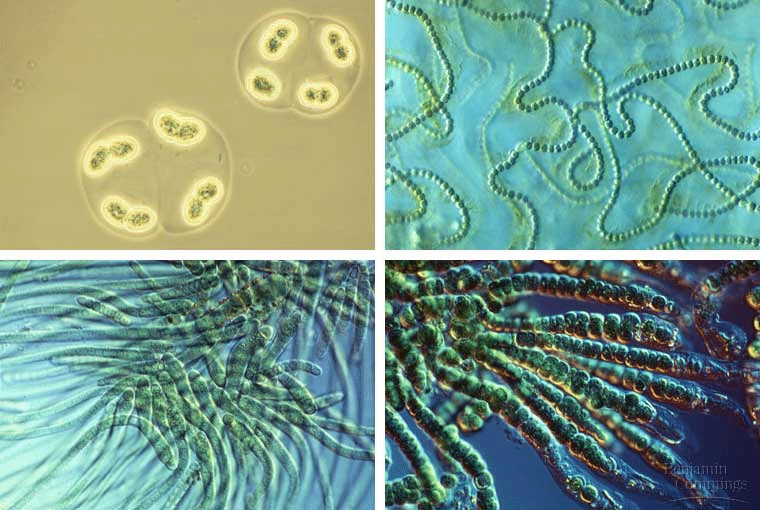 |
| Source : http://www2.ggl.ulaval.ca/personnel/bourque/intro.pt/planete_terre.html | Source : http://cas.bellarmine.edu/tietjen/Evolution/stromatolites2.htm |
A, B et C : sphéroïdes bactériens, D : filaments de cyanobactéries
Durant la journée, l'activité photosynthétique des cyanobactéries entraîne la précipitation de carbonates, qui sont englués avec d'autres sédiments par la substance visqueuse produite par les bactéries. Une fine couche de calcaire est ainsi formée. Durant la nuit, il n’y a pas de photosynthèse donc pas de dépôt de calcaire. La journée suivante, l'activité photosynthétique reprend, ce qui explique les couches concentriques apparaissant en coupe, dont chacune correspond à une journée.
Le dioxyde de carbone (dissous dans l'eau) est absorbé par les cyanobactéries pour leur photosynthèse, ce qui entraîne la formation de carbonate de calcium (CaCO3) en déplaçant l'équilibre de la réaction chimique suivante vers la droite :
2HCO3- + Ca2+ -> CaCO3 + CO2 + H2O
La séquence ci-dessous explique ce mode de formation des stromatolites actuels :
Source : "Planète miracle", épisode "La mer primitive" (NHK - Antenne 2, 1987)
Pistes d'exploitation